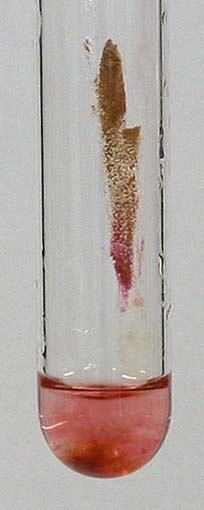
酸化マンガン(III)は、組成式がMn2O3で表される化合物である。
天然には、ビクスビ鉱(Bixbyite-(Mn))として産出する。
性質
二酸化マンガンを空気中で800℃以下で熱するとα-Mn2O3が生成する(より高い温度では酸化マンガン(II,III):Mn3O4が生成する)。γ-Mn2O3は水酸化マンガン(II)を脱水および酸化することで合成できる。数種のナノ結晶Mn2O3の合成法が報告されており、例えば、MnII塩の酸化またはMnO2の還元がある。
酸化マンガン(III)はアルカリセル中で酸化還元させることにより合成する。
酸化マンガン(III)はオキシ水酸化マンガン(III)(MnOOH)と混同してはならない。Mn2O3はMnO2を熱することで生成される化合物であるが、それとは逆に、MnOOHは300℃で分解してMnO2を生成する化合物である。
構造
Mn2O3は他の遷移金属酸化物と異なり、コランダム(Al2O3)構造をとらない。一般に、α-Mn2O3とγ-Mn2O3の二種が構造が知られているが、高圧条件ではCaIrO3構造が報告されている。α-Mn2O3はC型希土類セスキ酸化物の立方晶系鉄マンガン鉱構造をとる(ピアソン記号 cI80, 空間群 Ia3, #206)。 この鉄マンガン鉱構造では少量のFe3 の存在が斜方晶系のMn2O3を安定化させている(ピアソン記号 oP24,空間群 Pbca, #61)。
γ-Mn2O3は酸化物イオンが立方最密構造をとる酸化マンガン(II,III)のスピネル構造に相関している。これは、γ-Fe2O3とFe3O4の関係に似ている。γ-Mn2O3はネール温度39Kでフェリ磁性である。
出典